
Სარჩევი:
- ავტორი Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- ბოლოს შეცვლილი 2025-01-22 17:03.
The ნომერი დან ობლიგაციები რადგან ნეიტრალური ატომი უდრის ნომერი ელექტრონების სრული ვალენტურ გარსში (2 ან 8 ელექტრონი) გამოკლებული ნომერი ვალენტური ელექტრონების. ეს მეთოდი მუშაობს, რადგან თითოეული კოვალენტური ბმა რომ ატომის ფორმირება ამატებს კიდევ ერთ ელექტრონს ატომების ვალენტურ გარსს მისი მუხტის შეცვლის გარეშე.
უბრალოდ, რომელი ნაერთი შეიცავს კოვალენტურ ბმებს?
მაგალითები ნაერთები რომ შეიცავს მხოლოდ კოვალენტური ბმები არის მეთანი (CH4), ნახშირბადის მონოქსიდი (CO) და იოდის მონობრომიდი (IBr). კოვალენტური კავშირი წყალბადის ატომებს შორის: ვინაიდან წყალბადის თითოეულ ატომს აქვს ერთი ელექტრონი, მათ შეუძლიათ შეავსონ თავიანთი გარე გარსი ელექტრონების წყვილის გაზიარებით. კოვალენტური ბმა.
შეიძლება ასევე იკითხოს, რამდენი კოვალენტური ბმა შეიძლება შექმნას ატომში? წყალბადის ატომს შეუძლია შექმნას 1 ბმა, ნახშირბადის ატომს შეუძლია შექმნას 4 ბმები, აზოტის ატომს შეუძლია შექმნას 3 ბმა, ხოლო ჟანგბადის ატომს შეუძლია შექმნას 2 ბმა. მოდი დავშალოთ კითხვა. უპირველეს ყოვლისა, კოვალენტური კავშირი არის მიზიდულობის ძლიერი ელექტროსტატიკური ძალები ვალენტური ელექტრონების საერთო წყვილსა და ბირთვს შორის.
ამის გათვალისწინებით, რა არის კოვალენტური ბმის 5 მაგალითი?
კოვალენტური ბმის მაგალითები:
- წყალი. ამის მაგალითია წყალი. წყალი შედგება კოვალენტური ბმისგან, რომელიც შეიცავს წყალბადს და ჟანგბადს, რომლებიც აკავშირებენ ერთმანეთს H-ს შესაქმნელად2ო.
- ბრილიანტები. ბრილიანტი ნახშირბადის გიგანტური კოვალენტური კავშირის მაგალითია. ალმასს აქვს გიგანტური მოლეკულური სტრუქტურა.
- ვულკანიზებული რეზინი. კიდევ ერთი მაგალითია ვულკანიზებული რეზინი.
რა არის 3 ტიპის კოვალენტური ბმა?
The სამი სახის როგორც სხვა პასუხებშია აღნიშნული, პოლარულია კოვალენტური , არაპოლარული კოვალენტური და კოორდინაცია კოვალენტური . პირველი, პოლარული კოვალენტური , წარმოიქმნება ორ არამეტალს შორის, რომლებსაც აქვთ განსხვავება ელექტრონეგატიურობაში. ისინი არათანაბრად იზიარებენ ელექტრონის სიმკვრივეს.
გირჩევთ:
როგორ ვპოულობთ მოლეკულების რაოდენობას ქიმიურ ფორმულაში?
მოლების გამრავლება ავოგადროს მუდმივზე გაამრავლეთ მოლების რაოდენობა ავოგადროს მუდმივზე, 6,022 x 10^23, რათა გამოთვალოთ მოლეკულების რაოდენობა თქვენს ნიმუშში
როგორ ვპოულობთ ელექტრონების რაოდენობას დაუმუხტავ ატომში?

ატომური რიცხვი წარმოადგენს პროტონების რაოდენობას ატომის ბირთვში. დაუმუხტავ ატომში პროტონების რაოდენობა ყოველთვის უდრის ელექტრონების რაოდენობას. მაგალითად, ნახშირბადის ატომები მოიცავს ექვს პროტონს და ექვს ელექტრონს, ამიტომ ნახშირბადის ატომური რიცხვია 6
როგორია კოვალენტური ბმების სტრუქტურა?

კოვალენტური ბმა იქმნება, როდესაც ელექტრონების წყვილი ორ ატომს შორის არის გაზიარებული. ეს საერთო ელექტრონები გვხვდება ატომების გარე გარსებში. ზოგადად, თითოეული ატომი ხელს უწყობს თითო ელექტრონს ელექტრონების საერთო წყვილში
ჟანგბადის რამდენი პროცენტია ნაერთში CaCO3?

CaCO3*3Ca3(PO4)2-ის ელემენტარული შემადგენლობა. ელემენტის სიმბოლო მასის პროცენტი კალციუმი Ca 38,8874 ნახშირბადი C 1,1654 ჟანგბადი O 41,9151 ფოსფორი P 18,0322
რა ხდება იონურ ნაერთში?

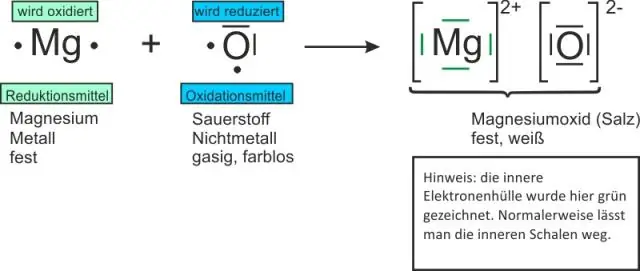
იონური კავშირი არის ატომებს შორის ვალენტური ელექტრონების სრული გადაცემა. ეს არის ქიმიური ბმის ტიპი, რომელიც წარმოქმნის ორ საპირისპიროდ დამუხტულ იონს. იონურ კავშირებში ლითონი კარგავს ელექტრონებს დადებითად დამუხტულ კატიონად გადაქცევად, ხოლო არამეტალი იღებს ამ ელექტრონებს უარყოფითად დამუხტულ ანიონად
