
- ავტორი Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- ბოლოს შეცვლილი 2025-01-22 17:03.
Როდესაც ელექტრონები გადავიდეს უფრო მაღალი ენერგეტიკული დონიდან ქვედაზე, გამოიყოფა ფოტონები და ემისია ხაზი ჩანს ში სპექტრი . აბსორბცია ხაზები ჩანს როდის ელექტრონები შთანთქავს ფოტონებს და გადადის ენერგიის მაღალ დონეზე. თუ ატომმა დაკარგა ერთი ან მეტი ელექტრონები , მას იონს უწოდებენ და ამბობენ, რომ იონიზირებულია.
ასე რომ, როგორ წარმოიქმნება სპექტრული ხაზები?
როდესაც ელექტრონები ხტება ქვემოთ n = 2 ორბიტაზე, ისინი ასხივებენ სპეციფიკური სიხშირის ფოტონებს (აქედან გამომდინარე ფერის), რომელიც შეიძლება ჩაითვალოს ემისია. ხაზები ემ-ის ხილულ ნაწილში სპექტრი . რაოდენობა სპექტრალური ხაზები ეს შეიძლება იყოს წარმოებული ფართოა ატომების, მოლეკულების და ორბიტალური გადასვლების პერმუტაციების გათვალისწინებით.
ანალოგიურად, რა ემართება რეალურად ელექტრონს ატომში, რათა წარმოქმნას სპექტრული ხაზი ემისიის სპექტრში? ან ემისიის ხაზი არის წარმოებული მიერ ა ატომი ``აღგზნებულ'' ენერგეტიკულ მდგომარეობაში --- ელექტრონი არ არის რაც შეიძლება დაბალ ენერგეტიკულ ორბიტაზე. დაიმახსოვრე წესი #3! ქვედა ენერგიის ორბიტაზე გასასვლელად, ელექტრონი უნდა დაკარგოს გარკვეული კონკრეტული რაოდენობის ენერგია.
შემდგომში ჩნდება კითხვა, რა იწვევს სპექტრული ხაზების გამოჩენას?
ყოფნა სპექტრალური ხაზები აიხსნება კვანტური მექანიკით ატომების, იონების და მოლეკულების ენერგეტიკული დონეების თვალსაზრისით. ემისია ხაზები ჩნდება როდესაც აღგზნებული ატომის, ელემენტის ან მოლეკულის ელექტრონები ენერგეტიკულ დონეებს შორის მოძრაობენ და უბრუნდებიან ძირითად მდგომარეობას.
რატომ აქვთ ელემენტებს განსხვავებული სპექტრალური ხაზები?
ემისიის სპექტროსკოპია. თითოეული ელემენტი აქვს განსხვავებული ატომური სპექტრი . წარმოება ხაზის სპექტრები ატომების მიერ ელემენტი მიუთითებს, რომ ატომს შეუძლია მხოლოდ გარკვეული რაოდენობის ენერგიის გამოსხივება. ეს მივყავართ დასკვნამდე, რომ შეკრულ ელექტრონებს არ შეუძლიათ აქვს ნებისმიერი რაოდენობის ენერგია, მაგრამ მხოლოდ გარკვეული რაოდენობის ენერგია.
გირჩევთ:
როგორ იღებენ და კარგავენ ატომები ელექტრონებს?

იონური კავშირი. ჩვენი უხეში, კონცეპტუალური განმარტების თანახმად, ქიმიური ბმები შეიძლება წარმოიქმნას ატომებს შორის ელექტრონების გადაცემით ან ელექტრონების გაზიარებით. როდესაც ატომები კარგავენ ან იღებენ ელექტრონებს, ისინი გახდებიან ის, რასაც იონები უწოდებენ. ელექტრონების დაკარგვა ატომს ტოვებს წმინდა დადებითი მუხტით და ატომს კატიონი ეწოდება
რა არის ატომის მუხტი, რომელიც იძენს ელექტრონებს?
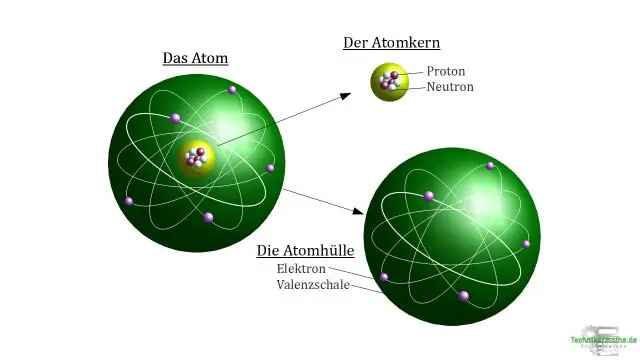
იონი არის ატომი, რომელმაც მოიპოვა ან დაკარგა ერთი ან მეტი ელექტრონი და, შესაბამისად, აქვს უარყოფითი ან დადებითი მუხტი. კატიონი არის ატომი, რომელმაც დაკარგა ვალენტური ელექტრონი და, შესაბამისად, აქვს მეტი დადებითი პროტონები, ვიდრე უარყოფითი ელექტრონები, ამიტომ ის დადებითად არის დამუხტული
ელექტრონებს აქვთ პოლუსები?

ელექტრონები მცირე ზომის მაგნიტებია. მათ ასევე აქვთ ჩრდილოეთი და სამხრეთი პოლუსი და ბრუნავენ ღერძის გარშემო. ეს ტრიალი იწვევს ძალიან პატარა, მაგრამ ძალიან მნიშვნელოვან მაგნიტურ ველს. ყველა ელექტრონს აქვს თავისი ღერძის ორი შესაძლო ორიენტაცია
როგორ შეიძლება იყოს განსხვავება სპექტრული ხაზების სიკაშკაშეში?

წყალბადის სპექტრში, ზოგიერთი სპექტრული ხაზები უფრო კაშკაშაა, ვიდრე სხვები, მათი ენერგიის დონის მიხედვით. როდესაც ელექტრონი გადახტება უფრო მაღალი ორბიტიდან, ფოტონისგან გამოთავისუფლებული ენერგია უფრო დიდი იქნება და მივიღებთ უფრო ნათელ ხაზს. ამრიგად, წყალბადის სპექტრში ზოგიერთი ხაზი უფრო კაშკაშაა, ვიდრე სხვები
რატომ არის სპექტრული ხაზები განსხვავებული თითოეული ელემენტისთვის?

თითოეული ელემენტის ემისიის სპექტრი განსხვავებულია, რადგან თითოეულ ელემენტს აქვს ელექტრონის ენერგიის დონის განსხვავებული ნაკრები. ემისიის ხაზები შეესაბამება განსხვავებებს მრავალი ენერგიის დონის სხვადასხვა წყვილებს შორის. ხაზები (ფოტონები) გამოიყოფა, როდესაც ელექტრონები ეცემა უფრო მაღალი ენერგიის ორბიტალებიდან ქვედა ენერგიებზე
