
- ავტორი Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- ბოლოს შეცვლილი 2025-01-22 17:03.
ჯამი ნომერი პროტონებსა და ნეიტრონებს ატომში ეწოდება მასობრივი რიცხვი . ატომური მასა არასოდეს არის მთელი რიცხვი ნომერი რამდენიმე მიზეზის გამო: ატომური მასა მოხსენებული ა პერიოდული ცხრილი არის ყველა ბუნებრივად არსებული იზოტოპის შეწონილი საშუალო. როგორც საშუალო, ნაკლებად სავარაუდოა, რომ მთლიანობა იყოს ნომერი.
ანალოგიურად, თქვენ შეიძლება იკითხოთ, რატომ არის პერიოდული სისტემა მოწყობილი ატომური რიცხვით მასის ნაცვლად?
ატომური ნომერი არის ნომერი პროტონები თითოეულის ბირთვში ელემენტის ატომები . რომ ნომერი უნიკალურია თითოეულისთვის ელემენტი . ატომური მასა განისაზღვრება იმით ნომერი პროტონებისა და ნეიტრონების გაერთიანებული.
გარდა ამისა, რატომ არ არის ბრომის ატომური წონა პერიოდულ ცხრილზე მთელი რიცხვი? ახსნა: ყველა ელემენტს აქვს იზოტოპების გარსი და ატომური მასა ციტირებულია Პერიოდული ცხრილი არის ცალკეული იზოტოპების შეწონილი საშუალო პირველი მიახლოებით ბრომი შედგება ორი იზოტოპისგან: 51% 79Br და 49% 81Br.
ასევე იცოდეთ, რატომ არის პერიოდულ ცხრილში ჩამოთვლილი ელემენტის ატომური მასა საშუალო შეწონილი მასის?
The ატომური მასა არის საშუალო შეწონილი ამის ყველა იზოტოპიდან ელემენტი , რომელშიც მასა თითოეული იზოტოპი მრავლდება ამ კონკრეტული იზოტოპის სიმრავლით. ( ატომური მასა ასევე მოიხსენიება როგორც ატომური წონა , მაგრამ ტერმინი " მასა "უფრო ზუსტია.)
როგორ განისაზღვრება მასები პერიოდულ სისტემაზე?, მაგრამ მათ აქვთ განსხვავებული მასა რიცხვები (პროტონებისა და ნეიტრონების ჯამური რაოდენობა), რაც მათ სხვადასხვა ატომს აძლევს მასები.
გირჩევთ:
სად არის ჯგუფი პერიოდულ ცხრილში?

ქიმიაში ჯგუფი (ასევე ცნობილია როგორც ოჯახი) არის ელემენტების სვეტი ქიმიური ელემენტების პერიოდულ სისტემაში. პერიოდულ სისტემაში არის 18 დანომრილი ჯგუფი; f-ბლოკის სვეტები (3 და 4 ჯგუფებს შორის) არ არის დანომრილი
რა არის 7 პერიოდულ ცხრილში?

ელემენტები წყალბადი, აზოტი, ჟანგბადი, ფტორი, ქლორი, ბრომი და იოდი არასოდეს განიხილება, როგორც ელემენტი თავისთავად. მეშვიდე, წყალბადი, თავისთავად გამორთულია პერიოდული ცხრილის „უცნაური ბურთი“
მთელი რიცხვები ყოველთვის არის თუ არასდროს რაციონალური რიცხვები?

1.5 არის რაციონალური რიცხვი, რომელიც შეიძლება დაიწეროს როგორც: 3/2, სადაც 3 და 2 ორივე მთელი რიცხვებია. აქ რაციონალური რიცხვი 8 არის მთელი რიცხვი, მაგრამ რაციონალური რიცხვი 1.5 არ არის მთელი რიცხვი, რადგან 1.5 არ არის მთელი რიცხვი. ასე რომ, შეგვიძლია ვთქვათ, რომ რაციონალური რიცხვი არის მთელი რიცხვი ზოგჯერ არა ყოველთვის. ამიტომ, ზოგჯერ სწორი პასუხია
რა არის ნატურალური რიცხვები მთელი რიცხვები მთელი რიცხვები და რაციონალური რიცხვები?
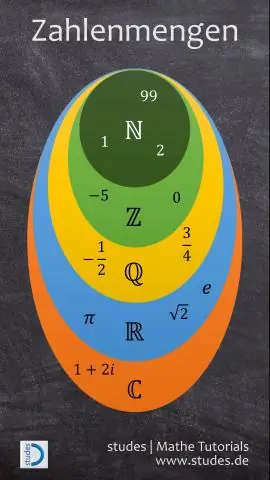
რეალური რიცხვები ძირითადად იყოფა რაციონალურ და ირაციონალურ რიცხვებად. რაციონალური რიცხვები მოიცავს ყველა მთელ რიცხვს და წილადს. ყველა უარყოფითი რიცხვი და მთელი რიცხვი ქმნიან რიცხვთა სიმრავლეს. მთელი რიცხვები მოიცავს ყველა ნატურალურ რიცხვს და ნულს
რა არის მთელი რიცხვები და რაციონალური რიცხვები როგორ გამოსახულია წერტილები კოორდინატულ სიბრტყეზე?

როგორც ვთქვით, წერტილები კოორდინატულ სიბრტყეზე წარმოდგენილია როგორც (a, b), სადაც a და b რაციონალური რიცხვებია. რაციონალური რიცხვები არის რიცხვები, რომლებიც შეიძლება დაიწეროს წილადად, p/q, სადაც p და q არის მთელი რიცხვები. a-ს ვუწოდებთ წერტილის x-კოორდინატს და b-ს წერტილის y-კოორდინატს
