
Სარჩევი:
- ავტორი Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- ბოლოს შეცვლილი 2025-01-22 17:03.
ნაბიჯები
- იპოვეთ თქვენი ატომის ატომური ნომერი.
- განსაზღვრეთ ატომის მუხტი.
- დაიმახსოვრეთ ორბიტალების ძირითადი სია.
- გაიგეთ ელექტრონული კონფიგურაციის აღნიშვნა.
- დაიმახსოვრეთ ორბიტალების რიგი.
- შეავსეთ ორბიტალები თქვენს ატომში ელექტრონების რაოდენობის მიხედვით.
- გამოიყენეთ პერიოდული ცხრილი, როგორც ვიზუალური მალსახმობი.
ანალოგიურად, რა ნაბიჯებია გადადგმული ელექტრონული კონფიგურაციის დასაწერად?
ნაბიჯები
- იპოვეთ თქვენი ატომის ატომური ნომერი.
- განსაზღვრეთ ატომის მუხტი.
- დაიმახსოვრეთ ორბიტალების ძირითადი სია.
- გაიგეთ ელექტრონული კონფიგურაციის აღნიშვნა.
- დაიმახსოვრეთ ორბიტალების რიგი.
- შეავსეთ ორბიტალები თქვენს ატომში ელექტრონების რაოდენობის მიხედვით.
- გამოიყენეთ პერიოდული ცხრილი, როგორც ვიზუალური მალსახმობი.
მეორეც, რა არის Subshell? ა ქვეჭურვი არის ელექტრონული ორბიტალებით გამოყოფილი ელექტრონული გარსების ქვედანაყოფი. ქვეჭურვები ელექტრონის კონფიგურაციაში ეტიკეტირებულია s, p, d და f.
ანალოგიურად, ისმება კითხვა, რა არის ჰუნდის წესი?
ჰუნდის წესი . ჰუნდის წესი : ქვეშელში ყველა ორბიტალი ცალ-ცალკეა დაკავებული ერთი ელექტრონით, სანამ რომელიმე ორბიტალი ორმაგად დაიკავებს, და ერთ დაკავებულ ორბიტალებში ყველა ელექტრონს აქვს იგივე სპინი.
რამდენი ელექტრონია თითოეულ გარსში?
თითოეული გარსი შეიძლება შეიცავდეს მხოლოდ ელექტრონების ფიქსირებულ რაოდენობას: პირველ გარსს შეუძლია გაუძლოს ორი ელექტრონი მეორე გარსი იტევს რვა (2 + 6) ელექტრონს, მესამე გარსს შეუძლია მდე 18 (2 + 6 + 10) და ასე შემდეგ. ზოგადი ფორმულა არის ის, რომ n-ე ჭურვი პრინციპში შეიძლება დაიჭიროს 2 (n2) ელექტრონები.
გირჩევთ:
როგორ წერთ ელექტრონის კონფიგურაციას MN-სთვის?

მეორე მხრივ, მანგანუმს აქვს ელექტრონული კონფიგურაცია 1s22s22p63s23p64s23d5 და კეთილშობილი აირის კონფიგურაცია [Ar]4s23d5, რის შედეგადაც წარმოიქმნება ერთი დაუწყვილებელი ელექტრონი თითოეულ 3D ქვეორბიტალში
როგორ პოულობთ ელექტრონის კონფიგურაციას ჟანგბადისთვის?

ჟანგბადისთვის ელექტრონული კონფიგურაციის ჩაწერისას პირველი ორი ელექტრონი წავა 1s ორბიტალში. ვინაიდან 1-ს შეუძლია მხოლოდ ორი ელექტრონის შეკავება, შემდეგი 2 ელექტრონი O-სთვის გადადის 2s ორბიტალში. დარჩენილი ოთხი ელექტრონი წავა 2p ორბიტალში. ამიტომ O ელექტრონის კონფიგურაცია იქნება 1s22s22p4
როგორ ასახავთ განტოლებას ეტაპობრივად?
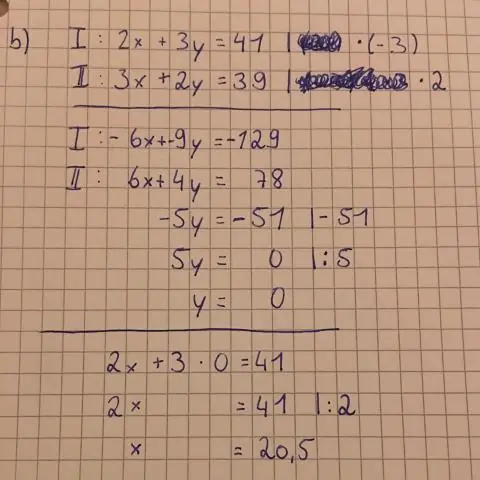
აქ არის რამდენიმე ნაბიჯი, რომელიც უნდა შესრულდეს: შეაერთეთ x = 0 განტოლებაში და ამოიღეთ y. დახაზეთ წერტილი (0,y) y-ღერძზე. შეაერთეთ y = 0 განტოლებაში და ამოხსენით x. დახაზეთ წერტილი (x,0) x ღერძზე. დახაზეთ სწორი ხაზი ორ წერტილს შორის
როგორ იპოვით ვერცხლის ელექტრონის კონფიგურაციას?

ძირითადი მდგომარეობის ელექტრონების კონფიგურაცია ძირითადი მდგომარეობის აირისებრი ნეიტრალური ვერცხლის არის [Kr]. 4d10. 5s1 და ტერმინის სიმბოლოა 2S1/2
როგორ აკეთებთ ფერდობს ეტაპობრივად?

სწორი ხაზის დახრილობის გამოთვლაში სამი ნაბიჯია, როდესაც არ არის მოცემული მისი განტოლება. ნაბიჯი პირველი: გამოავლინეთ ორი წერტილი ხაზზე. ნაბიჯი მეორე: აირჩიეთ ერთი იყოს (x1, y1) და მეორე იყოს (x2, y2). ნაბიჯი მესამე: გამოიყენეთ დახრილობის განტოლება ფერდობის გამოსათვლელად
