
- ავტორი Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:37.
- ბოლოს შეცვლილი 2025-06-01 05:04.
მიუხედავად იმისა, რომ ყველა მოლეკულა იზიდავს ერთმანეთს, ზოგიერთი ატრაქციონი სხვებზე ძლიერია. არაპოლარული მოლეკულები იზიდავს ა ლონდონის დისპერსია მიმზიდველობა; პოლარული მოლეკულები იზიდავს ორივეს მეშვეობით ლონდონის დისპერსია ძალა და უფრო ძლიერი დიპოლი - დიპოლი მიმზიდველობა.
ხალხი ასევე სვამს კითხვას, არის თუ არა დიპოლური დიპოლი უფრო ძლიერი ვიდრე ლონდონის დისპერსია?
ყველა მოლეკულა, პოლარული თუ არაპოლარული, იზიდავს ერთმანეთს ლონდონის დისპერსიული ძალები ნებისმიერი სხვა მიმზიდველის გარდა ძალები რომელიც შეიძლება იყოს. ზოგადად, თუმცა, დიპოლი - დიპოლი მცირე პოლარულ მოლეკულებში ურთიერთქმედება მნიშვნელოვნად არის უფრო ძლიერი ვიდრე ლონდონის დისპერსიული ძალები ასე რომ, პირველები ჭარბობენ.
შემდგომში ჩნდება კითხვა, რა არის ლონდონის დისპერსიული ძალების მაგალითები? ეს ლონდონის დისპერსიული ძალები ხშირად გვხვდება ჰალოგენებში (მაგ., F2 და მე2), კეთილშობილი გაზები (მაგ. Ne და Ar) და სხვა არაპოლარულ მოლეკულებში, როგორიცაა ნახშირორჟანგი და მეთანი . ლონდონის დისპერსიული ძალები ვან დერ ვაალის ძალების, ანუ სუსტი ინტერმოლეკულური ატრაქციონების ნაწილია.
ამის გათვალისწინებით, რა არის დიპოლური დიპოლური ლონდონის დისპერსია?
The ლონდონის დისპერსია ძალა არის დროებითი მიმზიდველი ძალა, რომელიც წარმოიქმნება მაშინ, როდესაც ელექტრონები ორ მიმდებარე ატომში იკავებენ პოზიციებს, რომლებიც ატომებს დროებით ქმნიან. დიპოლები . ამ ძალას ზოგჯერ ინდუცირებულს უწოდებენ დიპოლი -გამოწვეული დიპოლი მიმზიდველობა.
რა არის ყველაზე ძლიერი ინტერმოლეკულური ძალა?
წყალბადის კავშირი
გირჩევთ:
რა განსხვავებაა ოსმოსის დიფუზიასა და გაადვილებულ დიფუზიას შორის?

ოსმოზი ასევე ხდება, როდესაც წყალი გადადის ერთი უჯრედიდან მეორეში. მეორეს მხრივ, ხელშემწყობი დიფუზია ხდება მაშინ, როდესაც უჯრედის მიმდებარე გარემო არის იონების ან მოლეკულების მაღალი კონცენტრაციით, ვიდრე უჯრედში არსებული გარემო. მოლეკულები მიმდებარე გარემოდან უჯრედში გადადიან დიფუზიის გრადიენტის გამო
რა განსხვავებაა კორელაციასა და ჩი კვადრატს შორის?
ამრიგად, კორელაცია ეხება ორ ცვლადს შორის წრფივ ურთიერთობას. ჩვეულებრივ, ორივე უწყვეტია (ან თითქმის ასე), მაგრამ არსებობს ვარიაციები იმ შემთხვევისთვის, როდესაც ერთი დიქოტომიურია. Chi-კვადრატი ჩვეულებრივ ორი ცვლადის დამოუკიდებლობას ეხება. როგორც წესი, ორივე კატეგორიულია
რა განსხვავებაა კლიმატის ზონასა და ბიომს შორის?

კლიმატი კლასიფიცირებულია ატმოსფერული ტემპერატურისა და ნალექების მიხედვით, ხოლო ბიომი კლასიფიცირდება ძირითადად მცენარეულობის ერთგვაროვან ტიპებზე დაყრდნობით. კლიმატს შეუძლია განსაზღვროს რა ბიომი არსებობს, მაგრამ ბიომი, როგორც წესი, არ აკონტროლებს ან გავლენას ახდენს კლიმატზე იმავე გზით
რა განსხვავებაა მყარ და რბილ განათებას შორის?

განსხვავება რბილ შუქსა და მყარ შუქს შორის. მძიმე შუქი ქმნის მკაფიო, ხისტი ჩრდილებს. რბილი შუქი ქმნის ჩრდილებს, რომლებიც ძლივს ჩანს. მზიანი დღე მძიმე სინათლეა
რა განსხვავებაა ზოგად ქიმიასა და ორგანულ ქიმიას შორის?
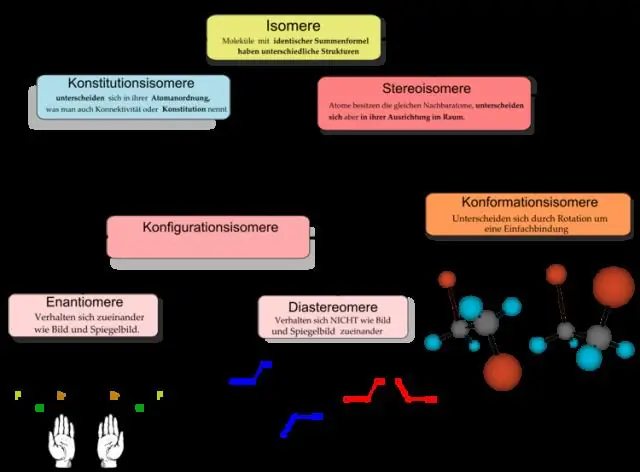
ორგანული ქიმია ითვლება ქიმიის ქვედისციპლინად. მაშინ როცა ზოგადი ქოლგა ტერმინი "ქიმია" ეხება ზოგადად ყველა ნივთიერების შემადგენლობას და გარდაქმნას, ორგანული ქიმია შემოიფარგლება მხოლოდ ორგანული ნაერთების შესწავლით
